유전자 특성에 따른 방사선 치료 효율 증진 물질 개발
환자의 유전적 특성에 따라 차별화된 암 치료를 가능케 하는 치료 효율 증진 물질이 개발됐다. 동일한 방법으로 방사선 암 치료를 받아도 효과가 달리 나타나는 환자들에 대해 이제는 유전자 검사를 통해 유전적 특성에 맞게 치료하고, 치료효과도 예측할 수 있게 됐다.
미래창조과학부(장관 최문기)는 방사선을 쪼여도 잘 죽지 않는 암 세포의 유전정보를 분석하여, 방사선치료 효율을 높이는 물질을 개발했다고 밝혔다. 방사선 치료는 수술 및 항암요법과 함께 암의 3대 치료법으로, 환자의 몸 상태가 수술을 받기 어렵거나 수술이 어려운 부위에 암이 생긴 경우 필수적으로 시행된다. 그러나 방사선에도 쉽게 죽지 않는 암세포들이 치료 효과를 높이는데 큰 한계가 되어 왔으며,
이를 극복하기 위해 방사선 치료 효과를 낮추는 유전자 또는 항암 유전자의 기능을 억제하는 물질 등에 대한 연구가 활발히 이루어져왔다.
한국원자력의학원(원장 조철구) 황상구 박사팀은 ‘HRP-3' 단백질이 암세포에 많이 발현되어 있으면 방사선 치료 과정에서 암세포가 잘 죽지 않는 것을 확인했다.
‘HRP-3' 단백질은 신경세포 분화에 중요한 역할을 하는 물질으로, 이번 연구를 통해 이 단백질이 폐암의 방사선 치료 효율을 저해하는 주요 인자라는 사실을 처음으로 밝혀내었다.
특히 연구팀은 'HRP-3' 단백질 제어를 통하여 방사선 치료 효과가 증진되는 기전을 환자의 유전적 특이성별로 밝혀내어, 맞춤형 치료효율 증진기술을 개발했다.
우선 ‘HRP-3’를 억제시키면 항산화 분자들의 감소로 생체 내 활성산소 제거가 원활하게 이루어지지 않고, 이에 과다한 활성산소가 암세포 사멸을 증진한다는 사실을 확인하였다.
지난해 9월, 암 억제 유전자로 알려진 ‘p53’ 단백질을 보유한 폐암 환자의 검체에서 이러한 기전을 확인하고 이를 이용한 치료효율 증진 물질을 개발, 국제 학술지에 발표 하였으며(BBRC 2013년 9월27일자*),
이번 후속 연구를 통하여 ‘p53’ 단백질을 보유하지 않은 폐암 세포주를 대상으로 ‘HRP-3’ 단백질을 이용한 치료효율 증진 물질을 개발하여 유전정보별 맞춤 치료 효과를 기대할 수 있게 됐다(BBRC 2014년 7월11일자**).
* (논문제목) Depletion of hepatoma-derived growth factor-related protein-3 induces apoptotic sensitization of radioresistant A549 cells via reactive oxygen species-dependent p53 activation. Biochemical and Biophysical Research Communications. 439(3): 333-339 (2013. 09. 27).
** (논문제목) Knockdown of hepatoma-derived growth factor-related protein-3 induces apoptosis of H1299 cells via ROS-dependent and p53-independent NF-κB activation, Biochemical and Biophysical Research Communications. (2014. 07. 11).
암세포에 대한 방사선 및 항암제 내성을 제어하는 치료효율 증진 물질은 2013년 9월 국내 특허에 출원되었으며, 2014년 7월 국제특허(PCT)에 출원될 예정이다.
* (특허명칭: 국내) 황상구, 윤홍식. HRP-3 억제제를 포함하는 방사선 또는 약물내성 암의 치료용 약학 조성물. 대한민국 특허출원 10-2013-0116450 (2013. 09. 30)
이번 연구결과는 「폐암 환자 방사선 치료 예후 예측, 바이오 진단키트 개발」 및 「표적 암 치료 신약 개발」등에 적용되어 향후 5년 내에 임상활용이 가능한 성과로 판단된다.
황상구 박사는 “방사선 치료를 받는 암환자의 유전정보를 분석하면 방사선치료 효과의 예측이 가능하다”며, “개개인의 특성에 맞는 최적 맞춤치료로 폐암의 방사선 치료 효율을 높이는데 기여할 것으로 기대한다.”고 밝혔다.
이번 연구는 미래창조과학부에서 지원하는 방사선기술개발사업의 일환으로 수행되었으며, 본 연구성과를 기반으로 연구팀은 2015년 2단계 사업에서는 항암제와 방사선의 병용치료 효과를 증진시키는 기술을 개발할 계획으로, 이를 통해 폐암 환자의 치료효율이 약 20% 이상 증진될 것으로 내다봤다.
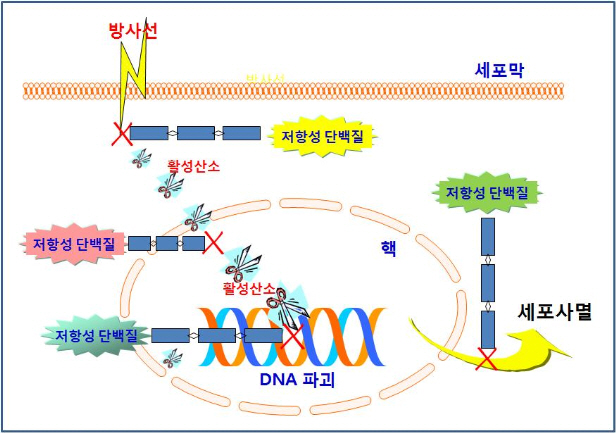
그림1.HRP-3단백질
HRP-3단백질의 정상세포 내 기능은 신경세포의 유사분열을 촉진하여 뇌의 신경계 발달에 기여함이 밝혀져 있으며, 간암세포에서 는 정상세포에 비해 발현양이 증가해 있다는 단순한 보고가 있다. 본 연구로부터 HRP-3가 폐암세포의 방사선치료 저항성을 일으키는 주요 인자임을 세계 최초로 밝혔으며, 관련된 신호기전을 분자수준에서 처음으로 규명하였다. 이러한 HRP-3단백질 제어에 의한 방사선 저항성 억제는 방사선치료의 민감성 증진에 직접적으로 기여할 수 있음.
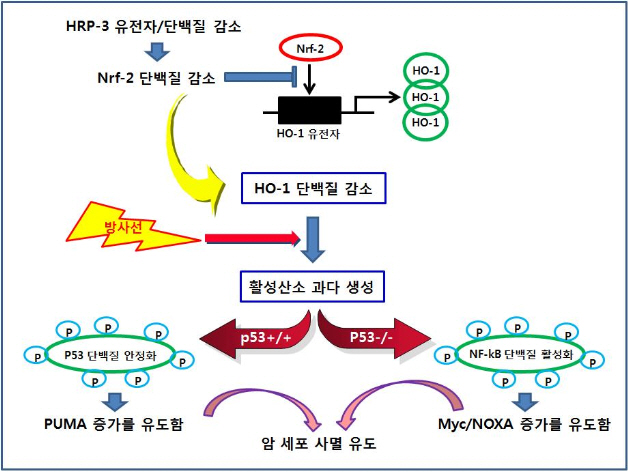
그림2.HRP-3억제에 의한 방사선치료 효율 증진 과정
연 구 자 이 력 사 항
1. 인적사항
○ 이름 : 황상구
○ 소속 : 한국원자력의학원 방사선의학연구소

○ 전 화 : 02-970-1353
○ e-mail : sgh63@kcch.re.kr
2. 학력
1994 부산대학교 박사 졸업
1990 부산대학교 석사 졸업
1986 부산대학교 자연대 생물학과 학사 졸업
3. 경력
2013 ? 현재 한국원자력의학원 방사선의학연구소 연구기획실장
2011 ? 2013 한국원자력의학원 방사선의학연구소 방사선암연구부장
2008 ? 2011 한국원자력의학원 방사선의학연구소 방사선종양형질연구팀장
2006 ? 현재 한국원자력의학원 방사선의학연구소 선임/책임연구원
2002 ? 2006 광주과학기술원 연구조교수
2000 ? 2002 창원대학교 유전공학연구소 전임연구원
1997 ? 2000 미국국립보건연구원 암연구소 객원연구원
www.newssports25.com
전재표 기자 su1359m@hanmail.net
기사 제보 및 보도자료/ 스포츠닷컴&추적사건25시
 신개념 패션 문화 축제 ‘패션코드 2014’ 개최
신개념 패션 문화 축제 ‘패션코드 2014’ 개최














